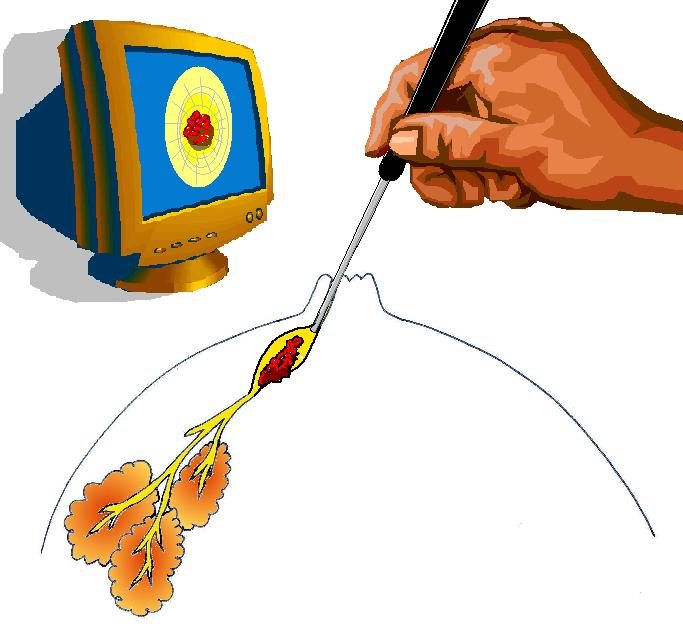
手術手技の実施
生検で診断が確定した線維腺腫を切除する際には、切開部位の選択と剥離方法に特に注意が必要です。切開部位を決める際には、以下の要素を総合的に考慮します:整容性/ 将来の授乳への影響/ 葉状腫瘍へのアップグレードの可能性(注:切除してみたら葉状腫瘍だったという可能性)/ 乳頭・乳輪複合体の感覚保持
線維腺腫の切除においては切除断端を陰性にすることは不要です。腫瘤は完全に摘出する必要がありますが、切断や細断は避けるべきです。手術中は頻繁に腫瘤を触診し、その位置を確認するとともに、腫瘤の一部を切断したり、不要に多くの正常組織を切除したりしないようにします。(これは前にも解説しましたが、外科医がきちんと取り切れたと判断していれば、病理の先生が顕微鏡で見て残っている可能性を示唆したとしても問題はない、ということです。ただ切除の際に、腫瘍をばらばらにして取り出したり、ちょっとずつ切って言ったりはするべきではない、ということです)
特に小児・思春期患者で線維腺腫を切除する場合、外科医は以下を心がける必要があります:正常な乳腺実質を温存すること/ 乳頭・乳輪複合体の周囲を避けて剥離し、乳腺芽および中心乳管を保護すること(注:これはある意味外科医の腕の見せ所です。こうしたことに配慮しながらきれいに腫瘍だけを残らず切除する、これこそ本領発揮です。)
非手術的管理
線維腺腫に対する薬物療法は、いくつかの研究で検討されています。これには無作為化比較試験も含まれます(注:きちんと正式な手続きを踏んでなされた研究もあるが、と前置きしています)。しかし、これらの治療法は臨床的効果が限定的であり、われわれのコンセンサスパネルは薬物療法の使用を支持しないという立場をとっています。
フォローアップケア
われわれ委員会は、生検で診断が確定した線維腺腫患者のフォローアップ方針を検討しました。結果として、以下について強い合意が得られました:
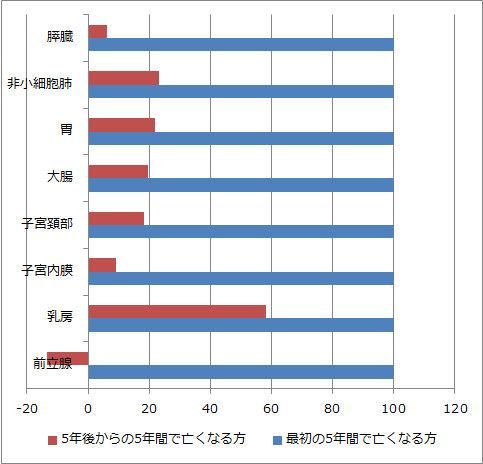
画像診断と病理診断が一致している線維腺腫に対しては、追加の画像検査や臨床フォローアップは不要である。これらの患者は、年齢に応じた通常の乳がん検診に戻ってよい。後ろ向き研究(247例、平均フォローアップ31か月)では、約80%の線維腺腫はサイズが安定していました。増大した症例のうち、切除されたもので、切除してみたら良性葉状腫瘍だったとなったいわゆるアップグレードは1例のみでした。
再受診の目安
以下の場合には、再度外科医への相談が推奨されます:線維腺腫が明らかに増大した場合/ 腫瘤のサイズが4〜6 cmに達した場合/ これらの状況では、外科的切除を含む対応方針を再検討します。(注:以前も触れましたが少なくとも米国では乳腺の自己チェックは高等教育に組み込まれており、しているのが常識です。)
多発性・両側性の病変
両側性または多発性で、画像上良性と判断される境界明瞭な腫瘤については、追加の画像検査や臨床フォローアップは不要であるとされています。この結論は、21施設で6,000件以上の検診データを解析した国際共同前向き研究によって裏付けられています。
まとめ
-
手術時は整容性・授乳機能・感覚温存に配慮。陰性マージンは不要。
-
薬物治療は効果が乏しく推奨されない。
-
生検で確定した線維腺腫は基本的に追加フォロー不要。
-
ただし、4〜6cmへの増大や急速な成長時は再評価を推奨。
-
多発・両側例は経過観察で問題なし。