乳がん術後に放射線治療を行うことで、局所の再発を極端に抑制することができることはよく知られています。特に乳房を温存する切除を行った後では、がんがあった部位周辺の取り残しを根絶するために、そしてリンパ節転移があった症例では、がんからリンパ節、リンパ節からその周辺へのがんの流れを焼いておくことで、局所再発をしっかりと抑制できます。
しかしたとえば乳腺の端のほうにあった小さな乳がんであっても、温存切除で残された乳腺すべてに放射線治療をする必要はあるのでしょうか?
乳がんがしこりが十分小さく、またリンパ節転移もなく、さらに切除後の病理のプレパラートでみても、がんのしこりの周辺にがんが広がる傾向が認められない場合、腋窩や、鎖骨の周辺への放射線治療はいらないのではないでしょうか?
また手術の前に抗がん剤による治療を受け、その後の手術でがんがほぼ消失してしまったことが証明されたときに、術後の放射線治療は本当に必要なのでしょうか?
今年 バルセロナで開催された第15回欧州乳がん会議(EBCC15)で発表された、10年間にわたるオランダの研究(RAPCHEM; BOOG 2010-03)によって、化学療法と手術後に、患者個々のリスクに合わせて放射線療法を行ったとしても、乳がんの再発率は低いままであることがあきらかになりました。
この研究では、化学療法と手術後に患者のリンパ節に乳がん細胞の痕跡が見られるかどうかに応じて、オーダーメイドの放射線治療が選択されました。リンパ節にがんの痕跡が残っていない女性の場合には、本研究では放射線治療を最小限に抑えるか、あるいは全く行わないことを選択しました。治療規模を縮小することで、もちろん患者の副作用を軽減することができます。
この研究は、オランダのマーストリヒト放射線腫瘍研究所(Maastro)で放射線腫瘍医研修中のフルール・モーリッツ医師によって発表されました。彼女は次のように述べています。「乳がん患者の多くにとって、最初の治療は化学療法です。これにより、手術前に腫瘍を縮小させ、体内に広がり始めているがん細胞を死滅させることができます。いっぽう放射線療法は、特に乳房全体ではなく腫瘍のみを切除する手術を受けた患者や、リンパ節にがんの兆候が見られる患者において、乳がんの再発リスクを低減することが知られています。この研究では、手術前に化学療法を受けた際にがんが良好な反応を示した患者において、放射線療法を縮小できるかどうかを検証しました。」
本研究には、2011年から2015年の間にオランダの17の癌センターで治療を受けた848人の患者が含まれました。各患者は、5cm未満の小さな乳房腫瘍を持ち、様々な検査において1つ、2つ、または3つのリンパ節に転移があると診断されています。
術前に化学療法を施行し、その後に手術を行った後、患者さんは3つの異なるリスクグループに分類されました。
リンパ節にがんの転移がないと診断された患者さんは低リスクと分類され、手術で腫瘍が切除され、乳房は温存された場合は残った乳房への放射線療法が行われ、乳房全摘術を受けた場合は放射線療法は行われませんでした。(筆者注:現在の通常の治療では、化学治療後に転移の兆候が消えていても、腋窩や、鎖骨周囲に放射線治療を加えます
リンパ節に1~3個の転移の兆候が見られた患者は中リスクに分類され、近くのリンパ節には照射せずに乳房領域のみに放射線療法を行いました。(筆者注:現在の通常の治療では、化学治療後に転移の兆候が残っていたら、確実に腋窩や、鎖骨周囲にも放射線治療を加えます。)
4つ以上のリンパ節に転移の兆候が残っていた患者さんは高リスクと分類され、乳房領域および周囲のリンパ節への放射線療法による治療が行われました。
その後の10年間で、追跡調査を完了した838人の患者のうち24人(2.9%)が、乳房、胸壁、またはリンパ節に再発したが、体内の他の部位への癌の転移は認められませんでした。低リスク群では291人中7人(2.4%)が再発し、中リスク群では370人中12人(3.2%)が再発し、高リスク群では177人中5人(2.8%)が再発しました。(筆者注:つまり差がありませんでした。)
マウリッツ博士は、「私たちの研究結果は、リンパ節の癌治療における化学療法の効果に応じて、副作用を抑えるために放射線療法の範囲を調整したとしても、乳房とその周辺領域における再発率が非常に低く、安心できる結果につながることを示しています。特定の患者グループでは、放射線療法を全く行わなくても、再発率が非常に低いことが確認されています」と述べました。
彼女は続けて、「本研究の大きな強みは、この患者群に対する放射線療法の個別化による効果を10年間にわたって初めて実証した点です。逆に本研究の限界というか、問題点は、研究対象となった患者のほとんどが腋窩リンパ節郭清術を受けたことです。この手術は10年前には一般的でしたが、現在の臨床現場ではあまり行われていません。(筆者注:腋窩郭清を全くせずに、つまりセンチネルリンパ節生検だけであったなら、同じ結果が出るかわからない、ということです。)また本研究では、放射線療法を受けた患者と受けていない患者を比較していません。(筆者注:本研究では全く行わなくても大丈夫かまでは検討していません。)
最終的な結論を得るには、米国/NSABP(ClinicalTrials.gov識別子NCT01872975)による無作為化試験の結果を待つ必要があります。結果は3年後に発表される予定です。」と述べました。

私がこの発表にひかれたのは、放射線治療をオーダーメイドする、という観点です。
いまはいい意味でも悪い意味でも、”ガイドライン”がガチガチに整備されていて、いわゆる主治医の判断が入り込む余地はなくなっています。これによって全国どこに行っても同じレベルの治療が受けられるようになりましたが、逆に患者さんと主治医が話し合って治療を決定していく、という要素がほぼなくなってしまっています。極端に言えば、AIに治療を決めてもらっても、主治医に決めてもらっても、変わりがないのです。誰がやっても一緒、いやむしろAIのほうが最新のガイドラインまですべて網羅しているので、優れている可能性があります。
ただ治療を受けるのは患者さんであり、人間であり、個別に訴えを持ち、治療に対する希望があります。
このブログでもたびたび述べていますが、たとえば閉経後乳がんじゅつごのホルモン治療は現在ほぼアロマターゼ阻害剤(AI)一択です。SERM(タモキシフェン)より明らかにがんの再発も、乳がんによる死亡も抑制することが分かっています。
でもAIは骨粗しょう症を引き起こします。関節痛、膝の痛みや、指のこわばり、腰痛などの原因になります。そして長期投与で骨がもろくなってしまうのです。
これは私自身の希望ですが、私は長生きはしたいですが、寝たきりになるくらいなら、早くいきたい、子供に迷惑をかけて長生きするのは嫌です。だから骨粗鬆が明らかになるまではAIでもいいですが、それが分かれば早急にむしろ骨を守ってくれるタモキシフェンに変更してほしい。
でもいまのところガイドラインには骨塩定量、つまり骨粗しょう症の検査結果に応じて、SERMとAIを使い分ける提案はされていません。
放射線治療も同様です。
私はNSMやSSM、つまり皮膚を温存して乳房は全摘し、インプラントで同時再建する術式をDirect to Implantと呼ぶのですが、この手術は温存切除であり、全的ではない、だから放射線治療を加えたほうがいい、と考えています。
しかし現状 ガイドラインでは放射線治療はいらないとされています。
ただ再建された乳房全体に放射線治療を当てると、再建が失敗することを最大として様々な合併症を引き起こします。ですので、たとえばがんがあった部位の周辺だけは放射線治療をしておく、であるとか、血流が少ないため合併症の原因になりやすい、乳腺のTop、乳頭付近だけは避けて周辺だけは当てておく、乳頭より内側にがんがあった場合には、胸骨周囲には当てておく、など、個別に応じて放射線治療ができればいいのに、と考えていた時期がありました。
リスクがコントロールできれば、NSM、SSMの対象とできる疾患も広がります。
この研究のように、医師の裁量部分を増やす動きは、いままでの反動として重要なのではないか、と考えています。ガイドライン一辺倒で、思考停止となるのではなく、患者さんという人間が、医師という人間と話し合いながら治療を模索していく、そういう時代に戻ってほしい、とそう願っているのかもしれません。
2026.04.06
「先生、サプリメントとか、飲んじゃだめですか?」
これは患者さんから本当によく尋ねられる質問で、昔からずっと変わりません。
がんの治療には、手術・抗がん剤・放射線治療などの「標準治療」があります。
これに対して、「補完代替医療(ほかんだいたいいりょう)」とは、簡単に言い切ってしまうならばこれらの治療以外の方法を指します。補完医療と代替医療があるのですが、その違いは、補完医療は標準治療と「一緒に使う」もので、ヨガ、アロマ、サプリメントなどです。代替医療は標準治療の代わりに使うもので、民間療法のみで治療しようとする場合です。重要なのは、代替医療だけでがんを治すことは、現在の医学では証明されていないという点です。というよりも証明されればそれは標準治療だからです。
最近 JAMAという雑誌に、この質問に対するしっかりした答えが掲載されています。これをここでまとめてみたいと思います。

はじめに
過去数十年にわたる乳がんの外科的および内科的治療における革新により、乳がんの全生存率は向上しています。手術、化学療法、放射線療法、内分泌療法、免疫療法などの従来の治療法は確実に進歩し、結果を出しているにもかかわらず、一部の患者さんは依然として補完代替医療(CAM)を選択し、施行しています。そこで本研究では 乳がん患者におけるCAMと生存率との関連性を明らかにしたいと考えました。
方法ですが、本研究では、2011年から2021年にかけて乳がんと診断された女性患者に関する国立がんデータベースのデータを分析しました。生存期間は、従来治療群、従来治療と代替医療併用群、および無治療群の間で比較されました。データは2025年5月から2025年12月にかけて分析されました。補完療法または代替療法については、非医療従事者によって実施される治療と定義しました。
その結果について、乳がんの女性患者2,169,202人のうち、2,157,219人(年齢中央値[IQR]、62歳[52-71歳])がサンプルに含まれました。
合計2,106,665人(97.6%)が従来療法を受け、273人(<0.1%)がCAMのみを受け、568人(<0.1%)がCAMと従来療法の併用を受け、49,713人(2.3%)が治療を受けていませんでした。
従来療法を受けた患者と比較して、CAMのみを受けた患者(調整ハザード比[AHR]、3.67、95%信頼区間、3.03-4.44、P < .001)または治療を受けなかった患者(AHR、3.53、95%信頼区間、3.48-3.58、P < .001)は死亡リスクが最も高いという結果になりました。
*ハザード比ですが、「従来療法を受けた患者と比較して、CAMのみを受けた患者ではハザード比が3.67でした」という表現によって、従来療法を受けた患者と比較して、CAMのみを受けた患者では3.67倍死亡する確率が高い、という意味になります(筆者注)
従来療法とCAMを併用した患者は、従来療法のみを受けた患者と比較して、内分泌療法(ステージIIでは40.7%対65.2%、P < .001)および放射線療法(ステージIIでは59.5%対36.6%、P < .001)を受ける可能性が低いということが分かりました。
従来療法とCAMを併用した治療を受けた患者は、従来療法のみを受けた患者と比較して、死亡率が高いという結果でした(AHR 1.45、95% CI 1.22-1.72、P < .001)。
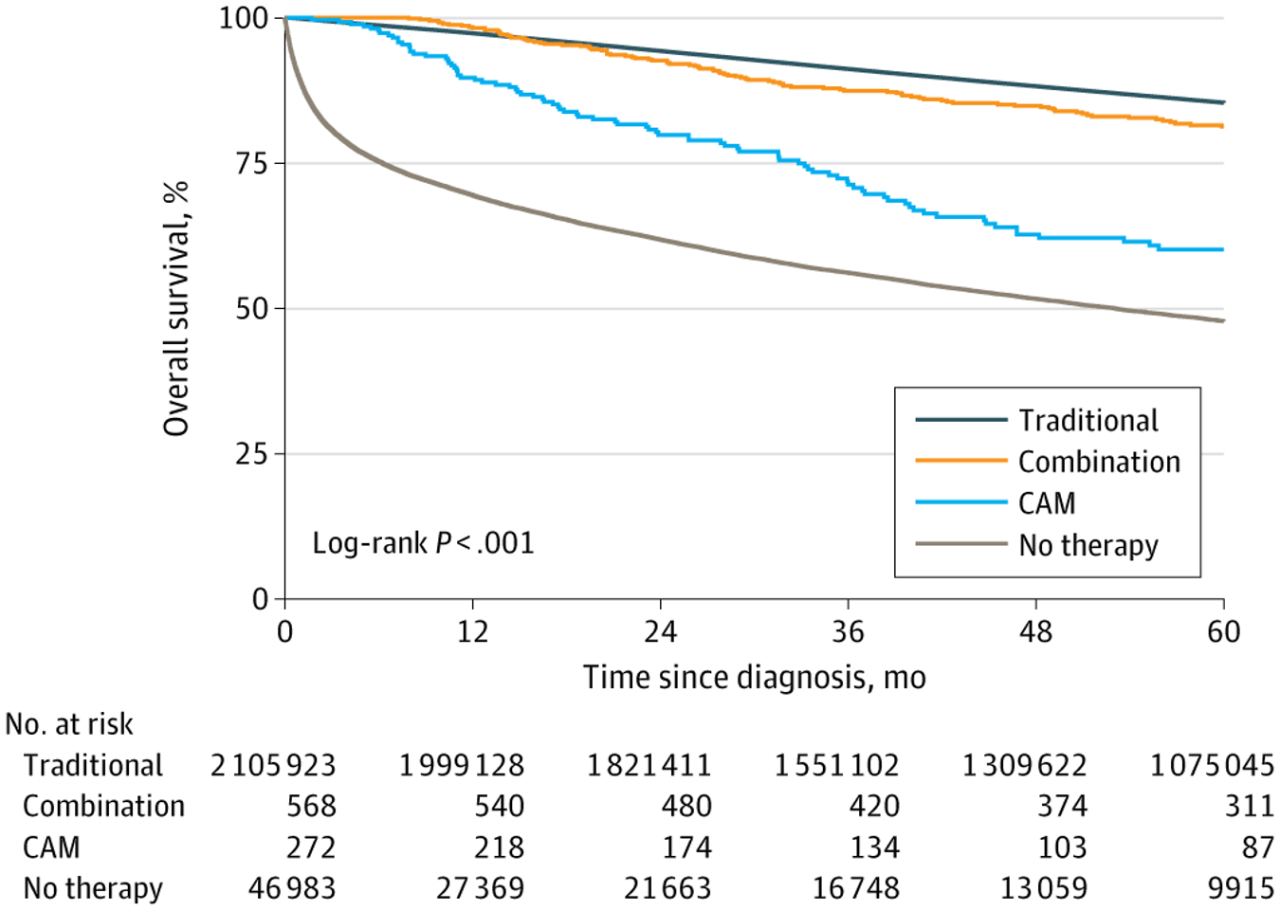
上のグラフはカプランメイヤー法によるもので、X軸で右に行くほど、時間が経過していることになります。12moと書いてあればそれは12か月経過した時点を指します。Y軸は生存率です。時間経過が0の時点では全員が生存していても、1年2年と経過するにつれ、亡くなる方が出て、生存されておられる方は減っていきます。つまり傾きが大きいグラフほど、生存率が低いという結果になります。
Traditional: 従来の標準治療
Combination: 標準治療と補完療法の併用
CAM: 代替療法のみ
No Therapy: 治療なし
今回の結果で、代替補完療法のみの患者さんが、治療なしよりも生存されていることには驚きました。そういう見方で見る方もおられるかもしれません。
ただ今回の研究は大規模ですが、それだけに様々な制限がかかっていると考えられます。
たとえば 今回の研究において代替療法とされた分類では、実は選択した多くの患者が見落とされている可能性があります。たとえば無治療とされても、実は補完療法を受けておられたり、標準治療のみとされていても、補完療法をこっそりされていたりです。その中には治療結果が大きく異なる患者もいるかもしれません。私の経験からしても、補完療法を併用されている方は0.1%程度では収まらないと思います。
ただそれを考えても、これだけの規模で比較すれば、小さな誤差は埋められると思います。
補完療法を受けられる方は、標準治療をきちんと完遂されない方が多く、そのため、治療成績が落ちる。
代替療法では、標準治療に成績では及ばない。
このことは今回の結果から明らかなのではないでしょうか?
2026.03.23
現在 人工知能(AI)を用いたマンモグラフィの読影が、進歩し、場合によっては人間の読影を凌駕する成績が出るようになってきています。少なくとも、人間の負担を減らし、発見率を上げることはすでに証明済みといってよく、確実な事実です。恐ろしいのはいったんAIの助けを借りるようになれば、人間の読影技術はそれによって進歩するのではなく、ほぼ確実に劣化することも指摘され始めています。いったん依存してしまえばもはや抜け出せないのです。
その問題はいつか触れるとして、最近、AIの助けを借りれば、定期的なマンモグラフィー検査で心血管疾患のリスクが高い女性を特定できる可能性があることが、ある後ろ向きコホート研究で示唆されました。
マンモグラフィの画像診断で、AIによって算出された乳房動脈石灰化の量が多いほど、内部検証コホートと外部検証コホートの両方で、その後の大きな心血管イベント(例えば狭心症、心筋梗塞など)のリスク増加と関連していました。例えば、高齢でリスクの高い外部検証コホートでは、乳房動脈石灰化が進行した女性は、追跡期間の中央値7年間で心血管イベントを経験するリスクが高くなっていました。
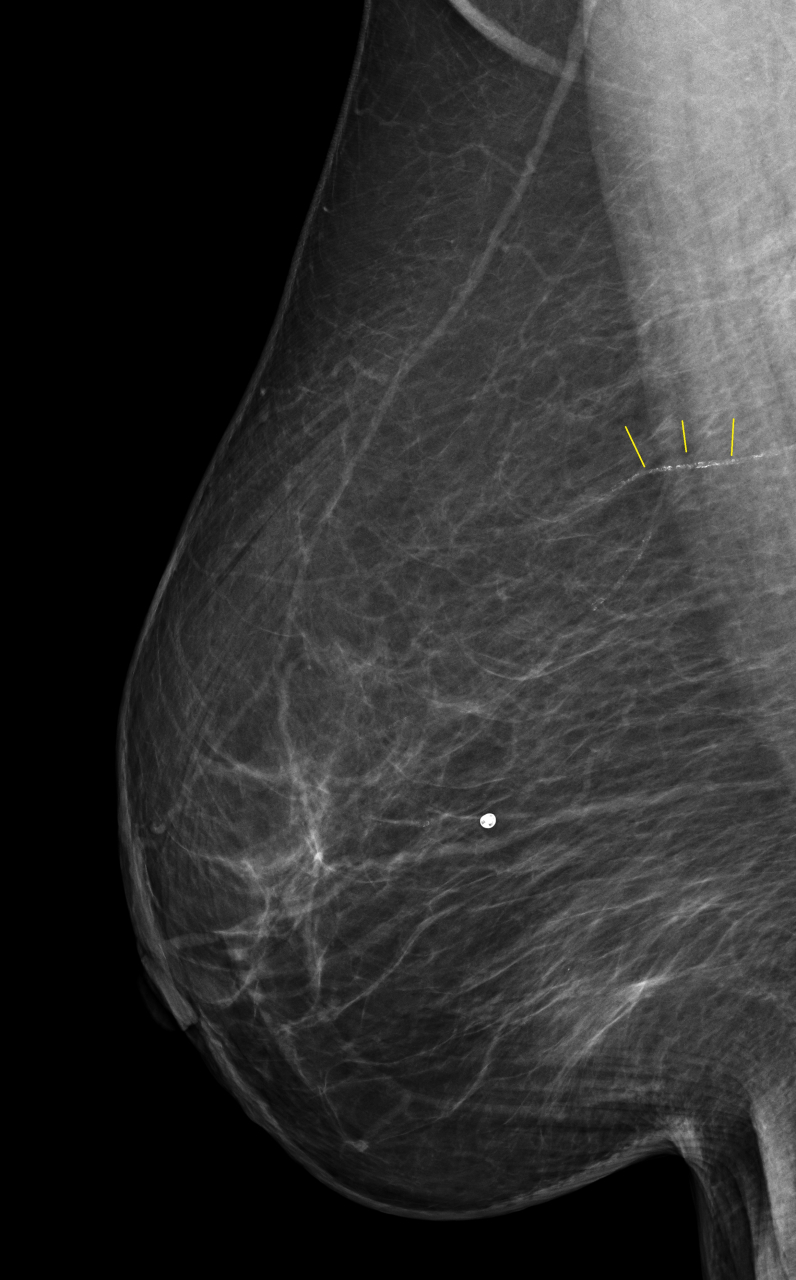
上記のMMGにおいて 黄色い線で示しているところは乳腺の動脈です。そこに沿って白い小さな点がびっしりと認められます。この動脈に”動脈硬化”が発生し、そこに石灰(カルシウム)が沈着することで描出されるようになったものです。
軽度の乳房動脈石灰化(>0-10 mm 2):調整済みハザード比 1.28(95%信頼区間 1.17-1.39)
*乳房動脈石灰化のない方と比べて心血管イベントを起こす可能性が1.28倍あるということ
中等度の乳房動脈石灰化(10~25 mm2 ):調整済みハザード比 1.79(95%信頼区間 1.55~2.06)
重度の乳房動脈石灰化(>25 mm2 ):調整済みハザード比 2.80(95%信頼区間 2.36-3.32)
「私たちの研究は、定期で行われるマンモグラフィー検査における、AIによる自動的な乳房内の動脈の石灰化の定量化が、大規模な多民族集団における心血管系有害事象の強力かつ独立した予測因子であることを示しています」と、アトランタのエモリー大学のハリ・トリヴェディ医師らは、この研究で示しました。
「この手法は、追加の放射線被曝なしに、定期的なマンモグラフィー検査中に心血管リスク評価を提供し、女性に対するより早期かつ効果的な予防医療を導く可能性がある」と彼らは結論付けました。
トリヴェディ氏らは、乳房内の動脈の石灰化が1mm²増加するごとに、主要な心血管イベントのリスクが2~3%有意に増加することを報告しました。この結果は、50歳未満の女性を含むすべての年齢層で有意であり、従来の危険因子やPREVENTリスクスコアとは無関係で、独立したものでした。(PREVENTリスクスコアは最近米国の学会において、汎用的な心血管リスク層別化ツールとして宣伝されたものです。)
「乳房内の動脈の石灰化の定量化は、PREVENTのような包括的なリスクモデルに取って代わることを意図したものではないことに留意することが重要です」と著者らは説明しています。「むしろ、乳房内の動脈の石灰化は、見過ごされがちなリスクの高い患者を特定し、かかりつけ医による正式な心血管リスク評価を促すための強力な指標として機能する可能性があります。」
「あなたがすでにマンモグラフィー検査を受けている女性の場合、この検査は、心臓の健康状態に関する重要な情報を提供し、コレステロール検査や投薬などの予防策について医師と話し合うきっかけにもなります」と、トリヴェディ氏はプレスリリースで述べています。「臨床医にとっては、現在見過ごされている心血管疾患リスクの高い女性を特定するための実用的な方法となります。」
マンモグラフィ検査は定期的に行われるものであるため、それと一緒に心血管リスクも評価するスクリーニングが可能であるならば、それには大きな意味があります。なぜなら、心血管疾患(CVD)は米国では重要な死亡原因の一つだからです。
米国では、女性における乳がんは一貫して診断は遅れがちで、かつ受けられる治療も十分とは言えない状態にあります。乳がんの早期発見のためのマンモグラフィーの受検率は40歳以上の女性において70%近くに達しています。
実際には、マンモグラフィーで乳房内の動脈の石灰化が指摘された場合、心血管疾患リスク因子の最適化と心不全予防を並行して行うべきであると、カリフォルニア大学サンディエゴ校のロリ・ダニエルズ医師は付随する論説で提言しています。
「重要なのは、乳房内の動脈の石灰化は、単純に心臓の冠動脈石灰化とイコールではなく、代用指標ではないということです」と彼女は書いている。「両者は相関関係にあるものの、病理学的には異なります。しかし動脈中膜に主に存在している乳房内の動脈の石灰化は、血管の老化と動脈硬化を反映しています。この区別は臨床的に重要です。なぜなら、これらの併存疾患は心室硬化、ひいては心不全、特に駆出率が保たれた心不全の発症と強く関連しているからです」と彼女は付け加えました。
トリヴェディ氏らは、この後ろ向き研究において、スクリーニングマンモグラフィーを受けた2つの医療システムに属する女性を対象としました。1つはエモリー・ヘルスケアの内部(自施設)検証コホート(n=74,124、平均年齢55.5歳)、もう1つはメイヨー・クリニックの外部(他施設)検証コホート(n=49,638、平均年齢59.5歳)です。主要心血管イベントおよびPREVENTのリスク変数は、電子カルテから抽出されました。主要心血管イベントには、急性心筋梗塞、脳卒中、心不全、および全死因死亡が含まれます。
乳房内の動脈の石灰化分析では左右両方の乳房を対象としましたが、各患者の最終結果としては、検出された値が最も高かった側の乳房のみを使用しました。最終的に、研究参加者の16.1%(内部コホート)および20.6%(外部コホート)で乳房内の動脈の石灰化が検出されました。
「本研究は、単一の包括的なリスクモデルをある施設で開発し、それを別の施設で外部検証するという従来の方法とは異なり、異なる集団における乳房内の動脈の石灰化の定量化の予後予測価値を検証することを目的として設計されました」と著者らは述べています。「言い換えれば、私たちの目標は、集団全体に適用できる『最適な』リスクモデルを作成することではなく、ベースラインリスクが異なる集団においても、独立した予測因子としての乳房内の動脈の石灰化の付加的な価値を示すことでした。普遍的なリスクモデルを開発することの難しさは、動脈硬化性心血管疾患やPREVENTリスク計算ツールが特定の集団にはうまく適用できないことを示すデータにも表れている」と彼らは付け加えました。
(この部分は難しいですが、こうした検証はある程度施設に依存していて、ある施設では成り立つけれども、他施設では成り立たない、がありうるということをできるだけ排除するように考えた研究です、と言っています。つまりどの施設であっても、このことは成り立つ、と言っているわけです。)
特筆すべき点として、この研究は人種的にかなり多様であったものの、アジア系、ヒスパニック系、ネイティブアメリカンの代表性は依然として限られていた。
「この研究のユニークなことは、実用的で直感的な報告指標である乳房内の動脈の石灰化を面積(mm²)として定量化した点にあります。あるなしの感覚的なものを、定量化し、それが心血管疾患のリスクにつながることが証明されました。これは単なる主観ではありません。物理的な単位を用いることで、ベンダー間の標準化を加速させ、再現可能な閾値を容易にし、実装ワークフローを円滑化できる可能性があります。(難しくいっていますが、つまりAIに組み込んでしまえば、どの施設でも心疾患リスクを同時に判定できるようになる可能性がある、」
「乳房内の動脈の石灰化の面積をわれわれは指標としましたが、最終的にどのような報告指標が採用されるかにかかわらず、女性の重要な死因である心疾患の予防を推進するために、女性が既に信頼を寄せている接点であるマンモグラフィ検診を活用し、乳房内の動脈の石灰化の評価を観察段階から実施段階へと移行させるべき時が来ています」と彼女は結論付けました。
2026.03.07
AI(アリミデックスやフェマーラ、アロマシン)なのか、SERM(タモキシフェン、トレミフェン)なのか、これが実はとても深い問題を含んでいるのです。
簡単に言い切れば、乳がんによる死亡を抑制してくれる効果はAIを100点としたらタモキシフェンは89点です。たしかに弱い。
そして副作用に関しては代表的なものを挙げるとタモキシフェンは子宮体癌、AIは骨粗しょう症になるでしょう。
え、副作用ががんなの、癌の再発を抑えるために他のガンが発生してたら意味ないじゃん。それならAIの圧勝でしょう。皆さんもそう思いますか?私は違う考え方をします。
これに関して、詳しくはこのブログで何度も触れてきましたが、子宮体がんはタモキシフェンを飲んでいなくても65歳以上であれば年間千人に一人は発症します。つまり0.1%です。飲んでいる方で多く見積もって1000人に二人なので0.2%と考えられます。
AIによる骨折の発生ですが、5年以上継続した場合、1.35倍になります。65歳以上の女性では10万人あたり年間約 646人 が大腿骨骨頭骨折を経験するとされていますので、千人に6人、0.6%とされます。もちろんこれは大腿骨骨頭に限定していますので、腰椎の圧迫骨折なども含めるともっと確率は上がります。
そしてもう一つ大事な情報ですが、タモキシフェンは骨を強くする、守る方向に働きます。AIが子宮体がんの確率を落とす効果があるかについては報告はありません。そしてタモキシフェンの子宮内膜への刺激は薬をやめればなくなります。つまり可逆的ですが、AIによって進んだ骨粗鬆症は、たとえAIをやめても原則元には戻せません。
現状 乳がん術後のホルモン治療は10年継続するように指導されている方は多いと思いますが、閉経後に限定した場合、その多くは60歳以上の女性になると思いますが、70歳になるまで10年ずっとAIで行くかどうかは、慎重でなければならない、と私は考えています。がんを抑制する効果は高くても、骨が脆くなってしまって、Quality of Life(=QOL) 生活の質、が下がってしまったら、元も子もない、と考えているからなのです。


ノースカロライナ大学チャペルヒル校ラインバーガー総合がんセンターのダニエル・R・リチャードソン医学博士(理学修士)らが最近発表した研究結果では、706人の進行したがん患者さんのうち、生存期間の延長を優先したのはわずか8.4%であったのに対し、QOLの維持を優先したのは71.7%で、残りはどちらでもないか中立だったと報告しました。
さらにクラスターランダム化試験の二次分析によると、進行がんを患う高齢患者は生存期間の延長よりも生活の質(QoL)の維持を優先する傾向があり、そして結局患者さんがどちらを希望し、優先しているかどうかに関わらず、こうした好みによって患者の転帰に差は生じなかったと言うこともわかりました。つまり事前の治療変更、またはグレード 3 ~ 5 の治療関連有害事象 (TRAE)、入院、死亡率などの下流の臨床結果がどちらを優先するかが異なる患者グループ間で比較しても結局差がなかったのです。それはおそらくそういった患者さんの志向によって、治療者が内容を変更することがないことも示していると考えられました。
編集者のメモオクラホマシティにあるオクラホマ大学ヘルス・スティーブンソンがんセンターの医学博士、公衆衛生学修士、経営学修士であり、JAMA Oncologyの副編集者でもあるライアン・D・ニップ氏は、「がん患者の大半は高齢者であり、この集団の QoL の優先事項を評価し、対処する研究をさらに進める必要がある」と書いています。「この研究が示したように、がんを患う高齢者は生存期間の延長よりもQOLの維持を優先することが多いのですが、私の知る限り、こうした患者のQOL向上を目的とした介入を評価した研究はほとんどありません」と彼は指摘しました。「こうした取り組みには、患者中心のケアを促進し、老年腫瘍学の分野で行われている革新的な研究に基づいた介入の開発と検証が含まれます。」

乳がん術後のホルモン治療に関しても、この研究と同じことが言えそうな気がします。
少なくとも65歳を超えた方に関しては、ホルモン治療を受けるかどうか、だけにとどまらず、その得られる効果、そして副作用も説明した上で、AIを選ぶか、SERMを選ぶか、話し合う必要があると私は考えます。そしてはそれはホルモン治療開始のその時だけではなく、たとえば1年ごとに副作用の出現やその程度を見極めながら、繰り返し話し合っていく必要があると思うのです。
そしてそうして患者さんの志向を聞いて、ホルモン剤を選んでいった場合と、医療側が最善と思われるホルモン剤を一方的に決めていった場合で、生存予後にどの程度の差が生じるのか、生じないのか? そしてその患者さんの人生の満足度にどのような影響が及ぶのか、ライアン先生の主張されているように、きちんと調査されるべきではないか、と私は考えます。
まとめ
進行がんを患う高齢者を対象とした研究では、生存期間の延長を優先したのはわずか8.4%であったのに対し、生活の質(QoL)の維持を優先したのは71.7%でした。
生存を優先した患者とQOLを優先した患者の間で、初期治療の変更や臨床結果に有意差はありませんでした。
これらのデータは、現在の腫瘍治療提供システムが患者の好みに対応できていないことを示唆していると研究者らは述べました。
私はこの結果をAIとSERMに準えて(なぞらえて)みました。
乳がんを患った高齢者を対象とした研究では、生存期間の延長を優先したのはXX%であったのに対し、生活の質(QoL)の維持を優先したのはZZ%でした。(もちろんまだそのデータはありません。)
生存を優先した患者とQOLを優先した患者の間で、初期治療の変更や臨床結果に有意差は〇〇した。(差が出るでしょうか? 出ないのでしょうか?)
このデータから、今後は特に高齢の女性乳がん患者さんにおいては、患者さんの志向を加味してホルモン剤を臨機応変に決定していく****(べきなのでしょうか? まだわかっていません。)
2026.02.10
最初に述べますが、このブログは必ず最後まで読める方が読んでください。抜き出しや、最初だけ読む、は厳禁です。誤って受け取られる可能性が高いからです。そのつもりで読んでください。
私のブログでも、また私の外来でも、また著作でも、講演でも、私はずっと乳腺の自己チェックの大切さを説き、そして勧めてきました。
その際に多くの方からされる質問は、「本当に 乳がんは触ってわかるのか?」です。
誤解を恐れずに驚くような解答をします。「乳がんは自己チェックではわからない」が答えです。
皆さんが、自分で触っていて、これががんだ、と確信できるようであればもはや遅い可能性が高いのです。だからがんを探そうとしてはいけないのです。もちろん、乳がんはどんどん大きくなってくるので、進行がんにまで至れば必ずわかります。
「本当に 乳がんは触ってわかるのか?」の質問には、「触っていたら早期で発見できるのか?」「乳がんで死なずにすむのか?」という内容が省略されています。自己チェックで乳がんは本当に早期発見できるか? 触っていれば、乳がん死は防げるか? これは現状では実は否定されています。「乳がん」を自己チェックする、という指導方法では死亡率は下げられないことがすでに分かっているのです。
この問題は非常に誤解を生みやすいのであえて触れないようにしてきました。ただとても大事なことなので、包み隠さず言わなければ真意が伝わらないことに気付きました。その真意とは、私は乳腺の自己チェックにおいて、
がんを探せとは言っていません。
先月と比べて変化を見落とすな、と言っています。
変化に気付く、そのためには同じ条件で比較する必要があります。また過去と比較しなければならないので、あまり間隔が空くと難しくなります。だから生理後に、定期的に必ずチェックする習慣をつけてください、と申しているのです。乳がんと確信できる段階まで待ってはいけないのです。変化の段階で気づく必要がある。
これは私の外来に来られた方のほとんどは聞いておられると思います。
もはや頭がこんがらがってきたと思います。だから避けてきた話題なのです。
それでもなんとかその解説をしてみようと思います。

定期的な乳腺の自己チェックを「教える/毎月やるよう指導する」よう介入することで、乳がん死は減少するか、について主要なエビデンスは、大規模なクラスターランダマイズ前向き試験が2本(中国・上海とロシア)で行われました。これらをまとめたCochraneレビューというものが公表されています。
Cochraneレビューでは、2つの大規模試験データから、乳がん死亡の減少は示されず、一方で害(良性病変の発見増・生検増)が増えるため、スクリーニングとしての自己チェックは推奨できないと結論づけています。また論考として Hackshawら(2003)が、生検が有意に増える(相対リスク 1.53, 95%CI 1.44–1.63)一方で、死亡減少は示されない、という要旨を示しています。
中国・上海(JNCI 2002 最終報告)では乳腺の自己チェック指導群 vs 対照群で、乳がん死亡は差がなかった(累積RR ≈ 1.04, 95%CI 0.82–1.33)一方で、良性乳房病変の診断が増える(=偽陽性→精査・生検が増える方向)という結果になりました。ロシア(St Petersburg/WHO関連の試験報告)でも、要約レベルではありますが、良性・悪性の検出や生検適応が介入群で増えることが示されています(=過剰精査方向)。
米国のUSPSTF(2009)(マンモグラフィ検診は2年おき、40歳から74歳まで、と決定した米国の公的機関)は「乳腺の自己チェックを教えることに反対(D推奨)」を明記しています。American Cancer Society(ACS)も、FAQで「BSEは(ルーチンとして)もはや推奨しない」旨を述べています。
ここまで読まれて皆さんもビックリされたと思います。
40歳を超えられた女性なら、昔乳がんの検診といえば、お医者さんのところに行って、”視触診”をされていたのを覚えておられる方もいると思います。現在ではそれは全くされていませんよね。
何度も言いますが、乳がんは大きくなってくるので、大きな乳がんは必ずわかります。医者が触っても、皆さんがご自身で触っても、です。しかしそれが早期でなければ、乳がん死の抑制は期待できません。つまり医者が触れば乳がんは見つかるのか 皆さんが触れば見つからないのか ではなくて、医者が触れば皆さんが触るより、早期、つまり乳がんを小さく見つけられる、だから乳がん死を抑制できる、その証拠がないと、わざわざ検診を受ける意味はないのです。
それは結局証明されませんでした。だから現在されていないのです。
そして同じく、皆さんに自己チェックを勧めても、早期がんで発見することはできなかった、むしろいらない検査ばかり増えた、だから推奨しない、となったのです。
それを知っていてなぜ私は乳腺の自己チェックを勧めるのか?
それは自己チェックの目標を変える必要がある、そして目標を変えれば有効である、と考えているからです。「がんを見つける」という指導から、「条件をそろえて変化に気付く」指導に切り替える必要がある、そうすれば早期がんで乳がんのしこりに気付けるのではないか、そして本当の乳がん以外のものを気にしてしまい、不要な検査を受けることも防げるではないか、と私は考えているのです。
だから「乳腺を自己チェックしていれば、がんはわかりますか?」という質問には、わかります、と答えてはいけないように考えています。それはその方は間違いなく、がんを探しているからです。私は、条件をそろえて比較することで、先月との違いに気付いてほしい、と言っているのです。
現在 30歳代の女性の乳がん死が増えてきています。そして30歳代の女性には検診を付与する公的なルールがありません。もし乳がんに罹患されても自分で気づくしか助かる道はないのです。
検診は行われていない、そして自分で触っても早期では見つからない、無駄な検査が増えるだけ、もしそうだとしたら30歳代で、もっといえば20歳代で、日本では60歳以上で乳がんになったら、もはや死ぬしかありません。運が悪かった、そうなります。
それは嘘です。検診で発見されていなくても、自分で早期で乳がんを見つけて医療機関を受診され、ちゃんと助かっている方も多いからです。
下の図を見てください。自分で見つけてこられた方の中でステージ I 早期がんの方の割合と、検診で見つかったがんの患者さんの中でのステージ I 早期がんの方の割合はそんなに違わないのです。ステージ 0はDCISといってしこりをそもそも作らないので、自分ではまず見つけられません。
自分で見つけても、検診でみつけても、ステージ Iの比率はそれほど変わらない。とすればその自分で早期で乳がんに気付いた人にどんな特徴があったのか、を見直す必要がある。早期で見つけられなかった人にどんな反省点があったのか、を見直す必要があると考えます。
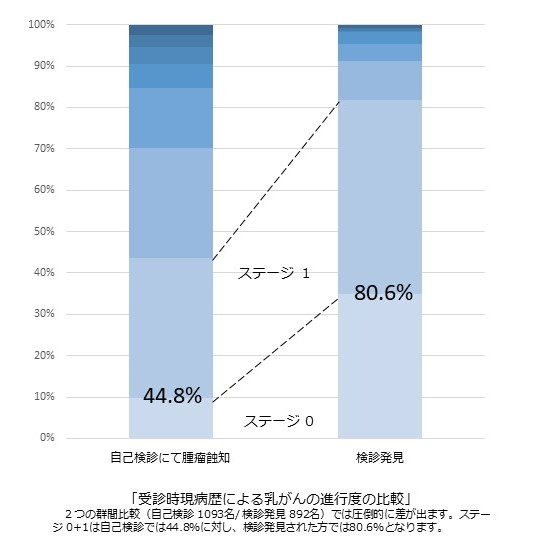
まず 検証の必要すらないことに、定期的にチェックする習慣があったのか? は言うまでもないでしょう。それ以外のヒントを提示したいと思います。
私のクリニックで、ビー玉チェックをされていて、乳がんに気付かれてこられた4人の患者さんについてお話ししたいと思います。ちなみにビー玉を見つけたと言ってこられて、乳がんではなかった方は2名です。当院では毎年述べ2万人強が受診されていて、乳がんは200名以上見つけています。その中の4名はまださみしい数ですが、考えてみてください。その4名の方は定期的に当院で乳腺の検診を受けていて、その検診と検診の間で自分で乳がんを見つけているのです。
その4名の方には共通の特徴があります。
まず検診を受けて異常なし、とされて、およそ3-5か月で、ビー玉に気付かれている。
(これは検診をしているものにも脅威です。まず前回の検診の際にもちいさながんは発生していたはずです。見つけられなかった、ということですので。)
マンモグラフィではすべて確認できませんでした。乳腺超音波検査で、訴えられているしこりの位置に異常を認め、測定上 5㎜が3名 8㎜が1名でした。8㎜だった方は乳腺の乳頭より下側でした。5㎜の方は乳腺が比較的薄い上側でした。
また非常に印象深いのは、来られた際のお話から、実は外来に来られるその1か月前から固い変化に気付いておられたそうです。でも自信がなかったからもう1か月待ってみた。生理が終わったので触ってみたら間違いなく、「大きくなっていた」から受診した、と言われたことです。乳がんではなかった2名の方はビー玉を見つけてすぐに受診された方でした。
逆に、最近の話題で 梅宮アンナさんが毎年検診を受けていたのに、進行がんとして発見された、ということがあります。北斗晶さんも同様です。お二人とも、毎年検診されていました。
つまり検診を受けることで安心してしまえば、乳がんがかなり大きくなるまで気づきにくくなることもまたあり得ると思います。
「検診を受けていても、いなくても」「生理後に条件をそろえて」 「定期的にチェックを行い」「乳腺の変化を見落とさない」これをそろえることで初めて自己チェックの効果が出てくるのではないか、私が生きている間に、38万人のデータまでは無理であっても、自己チェックを肯定する証拠が出せればと思っています。
大変長くなりました。
この内容は非常に誤解を生みやすく、今まで避けてきた話題です。しかしお付き合いいただけた方はわかっていただけたと思います。私は乳腺の自己チェックで早期がんを発見できる、と考えているのです。ただそれには正しい教育が不可欠で、間違った教育をすればしないほうがましな事態に陥ることも確実なのです。だからあえてこの記事を書きました。
もう一度 ここで強調しておきます。
私は、先月と比べて変化を見落とすな、と言っているのです。
皆さんが娘さんや、周囲の方に、自己チェックを勧める際、ぜひ、がんを探せ、という言葉を使わないでほしいのです。もしそう教えてしまえば、もしなにか異常があっても、痛くないから乳がんじゃないだろう、動くから乳がんじゃないだろう、と自分で判断して相談してくれない。変化があればその段階で気にしておく必要があるのです。自分でもはっきりがんだとわかったら遅い。「変化を見落とすな」「もし気づいたらすぐにお母さんに言いなさい」「相談しなさい」 これ一択です。
付記
実際のガイドラインとのズレ
国際的な医学ガイドライン(米国がん協会や英国NICEなど)は、近年では かつて推奨されていた自己触診(BSE:Breast Self-Examination)を「強く推奨しない」方向に変えています。代わりに「乳房に変化がないかに留意する(Breast Awareness)」という概念が重視されています。つまり、州法で教育が義務づけられている内容と最新の医学的推奨にはズレがあることがわかります。つまり米国でも法律上は自己チェックを勧める、となっているのですが、その内容はすでに、自己チェックから「乳房に変化がないかに留意する(ブレスト・アウェアネス)」に変化しているのです。
医師による触診による検診
これに関してはほぼ否定されたと思っています。医師の触診では過去と比較ができない、それが致命的に弱点です。微細な変化に気付けない。医師が前回の触診を覚えているはずがないからです。おそらく覚えていて比較ができるのは、こんなところに固いところが先月あったっけ、そう気づくことができるのはご本人だけでしょう。
2026.02.07
当クリニックは検診を目的に来院される方が主になりますが、それでもさまざまな乳腺にまつわる主訴をもって飛び込んで来られる方がおられます。そしてその中で最も多い主訴が”乳腺の痛み”です。その訴え方は様々で、それこそ「痛い」から始まって、「ちくちくする」、「違和感がある」、「なんか張るような感じがする」、など総じて程度に差があります。
その際に、「痛み止めが必要ですか?」と尋ねると、「それほどではない」と言われる方がほとんどで、ではなぜ受診されたのですか? といえば、「やはりがんが気になったから」となるのです。
これに関しては、その痛みはいつからですか? どこが痛みますか? 生理周期と関係がありますか? 波がありますか? 今までに経験したことのない痛みですか? といった質問をしていくことで原因がはっきりしてきます。この流れは以前このブログで整理していますので、もしよかったら先にそちらを参考にしてみてください。
乳腺痛について・・・その1
乳腺痛について・・・その2
乳腺痛について・・・その3
重要なことは、乳がんではなかった際に、ではなぜ痛いのか、が漠然と残ってしまうことにあります。そうなれば、この先も何か痛みがあるたびに気になってしまうので、結局問題が何も解決しません。
また娘さんや、職場の後輩の女性に、聞かれた際にもなにも参考になることが答えられず、不本意な思いをします。たとえば「もしかして、何かピルとか、生理不順でお薬とか飲んでいる?」と聞けたなら。実は不妊治療や、生理不順で使われるお薬の中には、副作用として乳腺の張りとか痛みがあるものが多いのです。それを知っていれば一つヒントになりますよね。
よかったらぜひ上の1,2,3を参考にしてみてください。今、現在読み返してみても、よくまとまっていて、付け足すことがありません(自画自賛で恥ずかしいですが)。皆さんのような一般の方が読んでいく中である程度原因が絞り込めるように書いています。できれば医療機関を受診して、必ず医師の診断を仰いでほしいですが、そうするとしても知識はあって邪魔になりません。

そして 「乳がんは痛むのか」についてです。
これにこたえるには、先に示した 乳腺痛について・・・その2 が解答になります。
神経の細胞は、急激に引き延ばされることで痛みの信号を出し、脳にそれを伝えます。
妊娠されたときに、あれだけおなかが大きくなっても痛みが少ないのは10か月かけて徐々に引き延ばされているからです。でも出産の際に会陰部は48時間ほどで一気に引き延ばされます。当然激しい痛みを伴います。
これが がん の場合であっても同じことが起こります。
もともとがん細胞は周辺の神経も冒し、破壊していくので痛みは出にくい傾向にあります。しかしがんが及んでいなくても、周辺には網の目のように神経は通っているので、そちらが信号を出します。
早期がんも、進行がんも、それを構成する細胞の数こそ違いますが、分裂速度そのものに差はありません。1㎜が2㎜に倍になるのも、10㎜が20㎜に倍になるのも理論的には同じ時間で起こります。しかしがんのしこりが大きくなることによって、その周囲に存在し、引き延ばされる神経にとって、1mmが2mm、と 10mmが20mmの変化、そのどちらが”急激”に引き延ばされているか、については言うまでもありません。だから乳がんも進行して、大きくなってくれば痛みを感じるようになる、が正しい回答になります。
ではどれくらいの大きさになったら痛みを感じるのか
これについてもすぐに想像がつきます。
現在9人に一人の女性が乳がんに罹患され、残念ながら早期では発見されず、大変多くの方が毎年亡くなっておられます。そこからわかることは少なくとも、十分に治癒できる早期の状態の乳がんでは痛みはない、だから気が付かない、ということが簡単に想像できるのです。
乳がんを早期で見つけるためには、痛みなどの自覚症状は全く参考にできない、のです。
乳がんが痛いかどうか、を気にされておられる方は、やはり痛みを参考にしてがんを発見しようとされていることは間違いないでしょう。でもおそらくそれががんによる痛みであるならば、自分で触って異変に気付く、固い、しこっている、しこりがあるなど、つまりがんの存在に気付くと思います。痛んでいるのなら、まず進行がんだからです。
痛くても、痛くなくても、常に、定期的に乳腺の状態を自分でチェックし、先月と変化しているところがないか、に注意を払っておくことが重要です。
痛みを無視しろ、と言っているのではありません。痛みをがんと結びつけて考えることはよくない、と言っているのです。痛みがあるからがんを調べる、のが間違いではありません。でも痛みがないからがんを調べない、のは間違いです。またがんでなければ痛みは調べない、もまた間違いです。他の重要な原因が隠れているかもしれないからです。
ややこしくなりましたね。
痛みの大原則ですが、もしがんで痛んでいるのなら、それは少しずつ悪くなっていきます。何にも治療せずに回復することは原則ありません。生理の周期と一致していたり、一過性にあったけれど、次第に回復してくるようなら、まずがんは関係ないでしょう。がんは治療することなしに自然に回復することはないからです。
そしてもし次第に増悪してくる痛みであるのなら、それはもしがんではない、と診断されても放置していてはいけません。他の病気の関与を疑って、たとえば総合内科、たとえば整形外科を受診するべきです。
下記に同じく乳腺痛について、動画にしました。よかったら見てください。

ラジオ波焼却療法は、肝臓がんではかなりの歴史があり、もちろん保険適応の標準治療としてすでに確立した治療方法になります。
これは簡単に言えば、腫瘍の中心部にラジオ波を放射できる先を持つ針を刺し、そこから発せられるラジオ波(簡単に言えばそとにラジオ波を放射できる電子レンジです)で、腫瘍を完全に焼いてしまおうという治療法です。この場合、検査で分かっている腫瘍よりもより広い範囲を焼くことで、周辺を含めてがん細胞を完全に焼き切ってしまうことを目的としています。
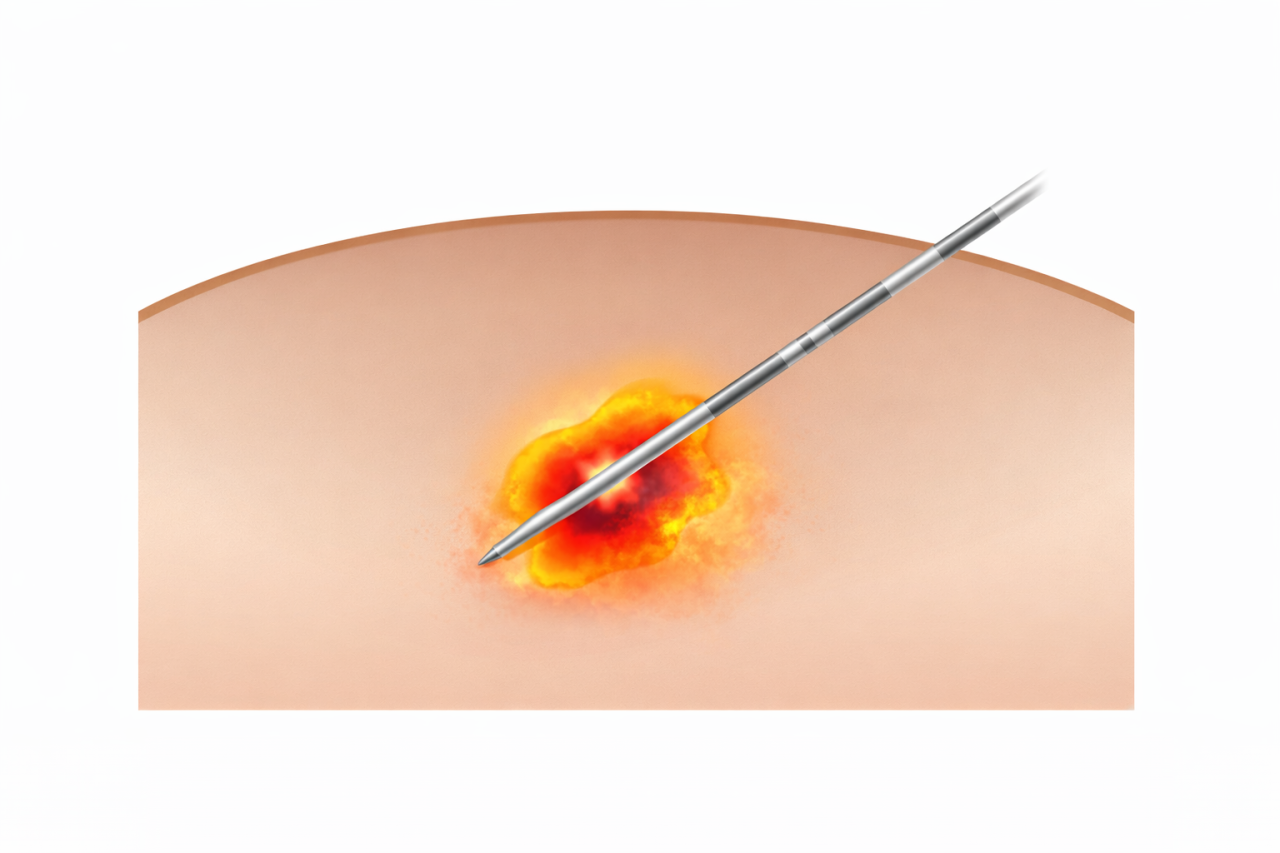
針の先の一部分からラジオ波が照射されます。それによって発熱が起こり、その周辺が球状に焼かれます。
肝臓がんを担当されている先生であれば施行したことがない方はおられないくらい一般的に広く行われている手技であり、安全性も危険性もほぼ確立されています。
それを乳がんに適応するものです。
上の図を見られればわかりますが、だいたい球状に焼けるので、その範囲内から逸脱する範囲にがんが及ぶ可能性があれば適応できません。したがってどうしても大きさの制限があります。
また切らないので、皮膚に傷は残りませんが、わずかにやけどを負う可能性はあります。また焼かれた腫瘍はそのまま固い瘢痕、つまりやけど後のケロイドとして残ります。がん細胞は死んでいるはずなのに、しこりは手術前から変わらずにそこにある、と感じられる患者さんがほとんどです。
ラジオ波による乳がんの治療は、日本を中心にして臨床試験が行われました。
肝臓がんでは確立した手技ではあるものの、果たして乳がんにそれを適応しても安全か? なにより乳がんはキチンとなおるのか? もともと手術で完全に治すことができるとされる早期の小さな乳がんが適応とされたため、その成績が手術に劣ることは許されません。
そして日本で厳密に行われてきたRAFAELO/PO‑RAFAELOなどの臨床試験および適応検討の記載から、早期乳がんのラジオ波治療はついに保険に収載されることとなりました。
その意味で私自身も早期乳がんは切らずに治せる、と確信はしていますが、実際にラジオ波治療の対象とされている条件はかなり明確かつ、厳密に規定されています。
先にラジオ波治療の適応とされる早期乳がんの定義を示します。
「画像・病理で確認された径1.5–2 cm以下の単発乳管癌(Stage 0–I, cN0)、EICや多発/多中心病変なし、術後に乳房照射と必要な全身療法を行うことを前提に、RFA単独で腫瘍を局所制御しうる症例」
これでは難しいので、下記に列記します。
早期乳がん(Stage 0–I)
TisN0M0, T1N0M0, T1N1miM0 が対象
腫瘍径が小さいこと(最大径 1.5–2.0 cm 以下 を条件としている。RAFAELO第III相試験では単発腫瘍で最大径1.5 cm以下を適格条件と明記 されている)
単発・限局性病変(単発の局在腫瘍(solitary localized tumor)であること)
乳管癌(ductal carcinoma) であること
びまん性石灰化や広範囲乳管内進展(EIC)を伴う症例は除外されている
画像上、境界明瞭で多発・多中心性の所見がないこと(乳腺超音波検査やMRIで辺縁明瞭、multifocal/multicentricを認めない早期病変が前提である)
画像診断上臨床的N0(一部のプロトコールでは、センチネルリンパ節生検で微小転移(N1mi)までは許容しているが、マクロ転移は除外される)
遠隔転移(M1)は当然ながら適応外。
乳房温存手術+放射線が原則可能な全身状態(麻酔・照射に耐えうること)であること。ちなみにラジオ波治療後は、必要に応じて乳房への放射線治療、ER/HER2・リンパ節・グレードに応じた薬物療法(内分泌/化学/抗HER2)を併用することが前提とされている。
不完全焼灼や残存病変が疑われた場合には、部分切除へ移行できることを前提とする。
まとめ
2023年12月に、早期乳がんに対するラジオ波焼灼療法(radiofrequency ablation: RFA)が健康保険の適用対象として認められました。現状 保険診療でRFAを受けられるためには、以下のような基準があります。腫瘍サイズが 1.5 cm 以下の限局性早期乳がん(腋窩リンパ節転移・遠隔転移なし)であること。患者さん本人がその治療に適格であり、医師が適正と判断すること。日本乳癌学会の術者・実施施設認定を受けた医師・医療機関で行われること。
実際にこの治療は 標準治療(手術)と同等の長期成績が確立している段階ではありませんが、短期成績は初期手術と同等と認められて保険適用されました。
制限はあるものの、2024〜2025年現在、多くのがん専門病院や大学病院で保険診療として保険の範囲内で治療が実施可能になっています。
当院で早期発見された乳がんの患者さんで、ラジオ波治療の適応ですよ、と言える方がおられます。また実際に切らずに治療される方も出てきています。厳密には切らないだけで、焼いてはいますが、せっかく早期で発見されたのに切るのですか? と言われる患者さんに、切らないでも治す方法が取れますよ、といえる時代になったと言えると思います。
2026.02.06
昨年 私のクリニックでは、「乳がん 自己チェックの始め方 母へ娘へ」という本を出しました。
これに合わせて、当クリニックの外来待合室では自己チェックの具体的な方法について、その内容を動画にし、常に流しています。そこではその際に使うビー玉も無償で提供しています。
ビー玉を使うのには大きな理由が3つあります。
1 使っているビー玉は1.7㎝です。乳がんは発見された際の病理学的なサイズ、つまり切除して顕微鏡で観察し、そのがんが及んでいる範囲が2㎝を超えていた場合、進行がんであると診断されます。早期発見であるためには何としても2㎝以内でなければなりません。ちなみに2㎝ぎりぎりで見つけても、それから受診し、検査し、手術にするまでの期間があるので、どうしても余裕を見る必要があります。ですので1.7cmなのです。
自己チェックで乳がんを早期発見するには、そのサイズを頭の中で理屈で分かっているだけではなく、具体的に自己チェックを行う手の”触覚”で知っておく必要があります。
ビー玉を乳腺に押し当てて、イメージトレーニングすることでそのことに対する感覚を覚えておく必要があります。
2 ビー玉を常に例えばお風呂場、たとえば鏡台など、目につくところにおいておけば、自己チェックを思い出しやすい。習慣になればもう忘れないですが、始めたばかりの際にはつい忘れてしまいます。お風呂の石鹸置き場など、どうしても目につくところにおいておけば忘れにくくなります。
3 お風呂場や洗面所など、鏡があって、家族全員が使う場所においておけば、たとえば娘さん、たとえばお母さん、など、自己チェックが必要なみんなにそれを伝え、思い出してもらうきっかけになることができます。
このビー玉を使って乳腺の自己チェックを始め、続けていく、というところが私のアイデアであり、この本の要点です。


本紹介:https://www.shounsha.co.jp/list/isbn/isbn978-4-910135-12-0.html
Shop: https://shounsha.stores.jp/items/67a9711dadce6619361be983
定価1,650円(本体1,500円+税)
この本にはビー玉が付録しています。
このように 私の勧める 自己チェックの始め方では、どうしてもビー玉が鍵になるため、そのやりかたの動画は作成したものの、このブログで公開することは今までしていませんでした。わざわざそのサイズのビー玉を探して購入する人手間が必要になれば、とにかく気楽に、そして正しく始めてほしい私の考えとすこしずれてしまうからです。また直接お会いしたことのない方に、これを勧めて本当に正しく伝わるだろうか、という疑問もありました。
それでもこれを読んでおられる方にも是非 乳腺の自己チェックを始めてほしい そういった強い気持ちはあります。
そこで今年の1回目のブログとして、この動画を公開します。下のQRコードを読み取っていただければご覧になることができます。一応このQRコードを見た方のみの限定公開になります。一般公開は今はしていないので、ご了承ください。
よろしければブログだけで私をご存じの方も、ぜひこれをご覧になり、正しいサイズ(1.7㎝)のビー玉をお求めになって、自己チェックを始めてください。
そしてもし、乳がんに罹患され、苦しい思いをされ、また今もされておられる方がおられましたら、自分の経験も踏まえて、周囲の大切な女性に自己チェックを勧めてあげてください。
普段から乳がんに関心を持っておられない一般女性に、いきなりマンモグラフィによる乳がん検診を受診するよう勧めることはかなり高いハードルになります。また40歳以下のクーポン検診の対象にはなっておられない、しかし乳がんにならないとは決して言えない若い娘さんをお持ちの方もおられるでしょう。そういった方にはまずは自己チェックを勧めてください。
歯磨きをきちんとされている女性は、やはりきちんと定期的に歯科受診をする傾向があります。
普段歯磨きもしない女性に(そんな女性はいませんが)、いきなり歯医者に行けと言ってもそれは難しい。だからまず自己チェックから勧めて、始めてもらうのです。
よかったらご検討ください。

このQRコードに入っているアドレスをご存じの方だけがみられる限定公開になっています。
2026年2月現在、一般公開はしていません。
ご了承ください。
2025.12.20
たとえば、高濃度乳腺と呼ばれる、乳腺の密度が高い方では、マンモグラフィ検診の有効性が落ちるだけではなく、乳がんのリスクそのものも高いことが指摘されています。乳腺の濃度は、若年者はもちろん出産経験のない方では高い傾向があります。現在のような少子化の時代では女性の大部分が高濃度乳腺科、不均一高濃度乳腺に属しているため、この問題は検診の現場においても、また検診をどのように受けていけばいいのかについても大きな影響を及ぼしています。
2025年12月 ドイツ・RWTHアーヘン大学の Christiane Kuhl 医師(MD, PhD) により、シカゴで開催された 北米放射線学会(RSNA)年次総会 において発表された、FDA(米国食品医薬品局)に最近承認された画像のみを用いるマンモグラフィ診断のための人工知能(AI)モデルを用いた研究結果では、米国および欧州から集められた24万件超の両側2Dスクリーニングマンモグラフィを対象とした解析において、AIによって高リスク群(National Comprehensive Cancer Networkの基準に基づいて分類)と判定された群は、平均リスク群と比べて乳がん発症率が4倍以上高かった(5.9% 対 1.3%)ことがわかりました。
Kuhl氏によれば、AIによるリスク評価では、「平均リスク女性において、観察された5年乳がん発症リスクが、設定された(想定)リスク値とほぼ完全に一致しており、同様にリスク上昇群でも良好な一致が見られ、さらに高リスク群と分類された女性では、はるかに高い発症率が観察されました」
さらに「乳房密度評価には問題があり、放射線科医によって判断が異なる」と述べています。
「AIによって自動化された乳房密度評価は、放射線科医による評価との相関が乏しく、従来の密度に基づくリスク認定は不正確であり、追加のスクリーニング方針を決定する目的には、おそらく有用ではありません」。(筆者注:我々医師が濃度が高いとか低いとか判断していますが、それと乳がんのリスクはそれほど相関していないことを指摘されています。AIで自動的に判断されたもののほうがはるかにリスク評価に役に立った、彼女はそう述べています。)
「AIモデルは、マンモグラフィから乳房密度をはるかに超える多くの情報を抽出することができます」とKuhl氏は続けました。「マンモグラフィにおける線維腺組織(乳腺実質)のテクスチャを解析し、それを用いて5年乳がんリスクをより包括的に推定できるのです」。
「このモデルは、人間の目では見えない乳房組織の変化を検出することができます。これは放射線科医には担えない作業です。検出や診断とは別次元のタスクであり、AIの力と画像に潜在している未活用の情報を活かすことで、まったく新しい医学の分野を切り開くでしょう」。
米国ではマンモグラフィ検診にAIが導入され、すでに実践に用いられていることがわかります。またAIによる乳腺実質そのものの評価によって、乳がんがその後に発生するリスクすら判定できる、つまり予防の観点から個別の検診スケジュールを提案するレベルにいたっていることも同時にわかります。
最近発表された研究においては、合計 42,236 件の 2D マンモグラフィー検査を受けた 42,100 人の女性で、単独の放射線科医による読影、2 人の放射線科医による読影、人工知能 (AI)による読影 (Transpara バージョン 1.7.0、ScreenPoint Medical)、そして ”AI を補助に使った一人の放射線科医による評価”を比較しました。
研究著者らは、 ”AI を補助に使った一人の放射線科医による評価”が、放射線科医二人による二重読影(51.7%)、放射線科医一人による評価(46.9%)、単独AI(48.6%)と比較して、最も高い感度(がんをがんとして発見する)(60.2%)を示したことを明らかにしました。また、 ”AI を補助に使った一人の放射線科医による評価”は、二重読影(97.7%)、放射線科医単独による読影(97.7%)、単独AI(97.8%)と同等の特異度(がんでないものをがんでないと否定する)(95.8%)を示しました。
研究者は「AIは、人間による評価では発見される乳がんを見逃す一方で、読影を行う放射線科医が見逃す乳がんを同程度検出します」と述べています。つまりAIは人間の読影を補填するのです。
このように今後はAIを用いて検診をし、さらに予防の観点からがんそのもののリスクすら評価を行っていく時代が来ています。しかしAIの導入はいいことばかりではありません。たとえば・・・
大腸内視鏡検査は、ポリープ(腺腫)の検出と除去を可能にし、大腸がんの発生を予防します。この分野においても、多くの試験において、大腸内視鏡検査にAIを活用することで腺腫の検出率が向上し、AI技術への関心が高まっていることが示されています。
しかしBudzyńらがThe Lancet Gastroenterology & Hepatologyに発表した論文によれば、大腸内視鏡検査を支援する人工知能(AI)の導入と日常診療における使用によって、AIの支援なしで大腸腺腫を検出する内視鏡医の能力の低下につながる可能性があることが示されました。
本研究は、2021年9月から2022年3月にかけて、ポーランドの4つの大腸内視鏡検査センターで実施されました。 AI非併用大腸内視鏡検査における腺腫検出率は、AI曝露前の28.4%(n = 226/795)からAI曝露後の22.4%(n = 145/648)へと有意に減少し、相対的に20%、絶対的に6%の腺腫検出率の低下に相当しました。AI併用大腸内視鏡検査では、腺腫検出率は25.3%(n = 186/734)でした。
検診分野へのAIの導入は、がんの発見率の向上に役立つばかりか、たとえば乳がんリスクの評価につながるなど、さまざまな福音をもたらしますが、検診に関与する医師に、けっしていい影響ばかり与えるわけではなさそうです。それに頼るあまり、どうしても”さぼって”しまい、日常の検診の中で同時に行なわれている”訓練”の密度も落ちるため、能力の低下につながるのです。これは簡単に予想できることでもありますよね。つまりいったんAIを導入すれば、AIのなかった時代には戻れない、ということです。
今後は その個人個人のたとえば家族歴、既往歴、そして出産歴などの評価に加えて、乳腺そのものの評価、生活習慣の評価などをAIを用いて評価して、その人その人に応じた検診のスケジュールや内容を提示していく時代が来ると思われます。
またたとえばBRCAという遺伝子を持たれたHBOC症候群の女性では、予防的に乳房切除を行うこともすでにわが国では保険適応とされており、乳がんの予防も可能になっています。
そこまでのことはできなくても、たとえばホルモン剤を予防的に投与され、引用している女性も海外では普通におられるようです。わが国ではまだそれは保険適応とされていませんし、それを管理する医療施設も整っていません。
AIの力を借りて、個別にリスクを”評価”し、その方に応じた”検診”を提示、施行し、可能であれば”予防”する、ことがすでに試みられ始めています。
2025年はお世話になりました。
このコラムを読んで、遠方からセカンドオピニオンに来てくださった方もおられました。その方々からいただいたお言葉も大変励みになりました。
来年も張り切って記事を書いていきますので、よろしくお願い申し上げます。
前回の結論は「乳がん検診はリスクに応じて2年おきでも問題はない」という結論でした。ただこのブログでも何度も述べてきましたが、米国の乳がん検診は、そして我が国の乳がん検診の現状も、”一律に2年に1回”です。ですので、この試験において、比較対象群として ”一律に毎年” を置いたのは現状を反映していません。ですので、この試験を計画している医師は、「リスクがない方でない限りは2年に1回ではなく、毎年検診を受けておくべきだ」ということが証明したかったのではないか、とも考えられます。ではそのリスクとは何でしょうか。
乳がんは、アメリカで女性に最も多く診断されるがんであり、今もなおがんによる死亡原因の上位を占めています。2025年には、約32万人の女性が乳がんと診断され、約4万人が亡くなったと推定されています。これは、女性が一生のうちに約8人に1人の割合で乳がんになることを意味します。このような状況は、予防・検診・治療のさらなる改善が必要であることを示しています。
乳がん検診は、一部のがんを早期に見つけ、治療しやすくするという利点があります。しかし、乳がんそのものを予防するわけではありません。
また、検診には次のような害もあります。実際にはがんでないのに「疑いあり」とされる(偽陽性) 一生問題にならないがんを見つけてしまう(過剰診断)(筆者注: これは驚かれた方も多いと思います。たとえば非浸潤がん(DCISやLCIS)と呼ばれるStage 0の乳がんは、それが最終的に命を奪うような皆さんの知る浸潤がんに、どの程度のものが移行するのか、どういうものが移行するのか、何年で移行するのか、よくわかっていないのです。こうしたStage 0乳がんの中には一生そのまま、生命の脅威にならずにおとなしくしているものもいることが分かっています。ただ実際に移行するものもあります。結局それを見分ける方法が見つかっていないので、現状では原則切除となっているのです。
ほかにもたとえば甲状腺にできる乳頭がんという種類のがんは、かなりの確率で一生そのままであることが分かっています。たとえば未分化転化など、リスクを理解し、受け入れてもらったうえで、そのまま切除せず、経過観察されている方もおられるがんです。
ただ、いまのところはDCISを経過観察で対応するのは標準治療とは言えず、臨床試験段階の域は出ていません。)
これらは、不安や不要な検査・治療、費用の増加につながります。
つまり、検診は多ければ多いほど良いとは限らないのです。
これまでの乳がん検診は、「○歳になったら全員同じ方法で」という年齢を基準にした一律のやり方が中心でした。しかし、乳がんになるリスクは人によって大きく異なります。
アメリカ女性の平均的な生涯リスクは約13%ですが、これはあくまで平均値です。実際には、多くの女性は平均より低いリスクであり、一部の女性は非常に高いリスクがある、といった風に偏りがあります。
特にリスクが高いのは、BRCA1などの遺伝子変異を持つ人、非浸潤性小葉がん(LCIS)の既往がある人です。
リスクが低い人では、検診による害(過剰診断や偽陽性)の影響が相対的に大きくなります。そのため、検診を控えめにする合理性があります。一方、リスクが高くなるほど、検診でがんを見つけられる可能性が高くなり、より頻回・別の方法の検診が有効になります。
リスクに基づく検診とは、検診を始める年齢 検診の間隔 使用する検査方法を、その人の乳がんリスクに合わせて調整する考え方です。これにより、早期発見の利点を保ちつつ、検診の害を減らすことが期待されます。
今回紹介したJAMAでは、Essermanらが、WISDOM試験という無作為化臨床試験の主要な結果を報告しています。これは、リスクに基づく検診の効果を実際の医療現場に近い形で検証した、初めての試験です。さらにこの研究は、個人に合わせた乳がん予防にもつながる可能性を示しています。
WISDOM試験では、女性を以下の2つのグループに分けました。1 リスクに基づく検診 と 2 毎年一律にマンモグラフィを受ける従来型検診(筆者注:繰り返しになりますが現状 わが国では2年おきですし、米国でも推奨は実は2年おきです)です。
リスク評価には、1 個人のリスク因子 2 家族歴 3 遺伝子検査 4 乳腺の密度 が含まれていました。(ご自身の乳がんリスクに関して知りたいと感じられた方は、乳腺科のDrに一度は検診を受けに受診し、尋ねてみられることを勧めます。)
最もリスクが高い人には、6か月ごとにマンモグラフィとMRIを交互に実施。最もリスクが低い50歳未満の人には、検診を行わないという方針が示されました。
主な評価項目は、進行乳がん(ステージIIB以上)が増えていないか 針で突いたり、一部を採取するなど、侵襲を伴う検査=生検の回数が減ったか でした。
約28,000人の女性が参加しましたが、参加者の集まりが想定より遅く、追跡期間が延長されました。
リスクに基づく検診グループでは、約10%が「高リスク」と判定され、そのグループにおける実際のがんの発生率は、予想通り、リスク評価と一致していました。
低リスク群でも、高リスク群でも、発見された際に進行乳がんであった割合は、従来型検診と比べて悪化はせず、低リスク群では2年おきの検診でも問題ないとする安全性は確認されました。
(筆者注:本来米国の検診は2年おきです。ですので対象は毎年一律に検診する、ではなく2年おきに一律に検診する、にするべきでした。ただ2年おきだともともと多くの進行がんが見つかることが分かっているので、1年おきを比較対象とするいびつな研究になっています。ですので、この結果は、高リスクの人を問題にするよりも、「低リスクの方では2年おきの定期健診で問題ない」という結果だとみるべきなのです。)
しかし、生検の回数は減りませんでした。
WISDOM試験の大きな強みは、検診を個別化するだけでなく、予防につなげられる可能性を示した点です。(この表現は誤解を生みやすいと思いますが、重要なことを述べています。検診にがんを予防する効果はありません。こうしたリスク評価を検診時にすることで、リスクが高いとされた女性がその後の生活習慣を改善する効果が副次的に生まれ、そのことで乳がんだけではなく、様々な病気が予防される、ということが認められた、と言っています。つまり検診そのものよりも、その女性のリスクを評価し、啓蒙することが、大きな予防効果を生む、ということが今回わかったのです。)
乳がんの主な生活習慣リスクには、閉経後の肥満 飲酒 運動不足 授乳経験の少なさ ホルモン剤の使用があり、これらは乳がんの最大25%に関係するとされています。
本試験では、リスクが高いと知らされた女性で、飲酒量の減少や運動量の増加がみられました。
一定以上のリスクがある女性では、タモキシフェン ラロキシフェン アナストロゾール エキセメスタン といった薬により、乳がんリスクを30~65%下げることができます。効果は治療終了後も長く続きます。これらは、個人にも社会にも非常に有効で、費用対効果の高い予防法です。(筆者注:これはわが国では保険適応とされていません。また乳がん患者さんにしようされるホルモン剤で、乳がんを予防する、という考え方はまだ一般まで普及していません。もちろん副作用もありますので、厳重な管理が必要な予防対策ということになります)
ガイドラインでは推奨されているにもかかわらず、実際に予防薬を使っている人は非常に少ないのが現状です。WISDOM試験でも、使用率はわずかでした。
その理由として、自分が高リスクだと知らない 医師も患者も予防薬の存在を知らない 専門的な相談体制が不足している といった問題があります。
今後に向けて 乳がん予防は主にかかりつけ医が担いますが、専門医の関与があると予防薬の使用率は大きく向上します。理想的には、専門医が初期説明と導入 かかりつけ医が継続管理 という連携体制が望まれます。(これも日本と異なる点になります。疾患に罹患する前に、健康な状態でかかる、予防や、検診を担当するかかりつけ医がいる、ということです。)
肺がん検診が禁煙支援と結びついているように、乳がん検診も予防と一体化すべきです。
WISDOM試験は、リスクに基づく乳がん検診が安全で実施可能であることを示しました。ただし、実際の効果を最大限に引き出すには、検診と予防を意図的に統合する仕組みが必要です。
ご予約専用ダイヤル
079-283-6103